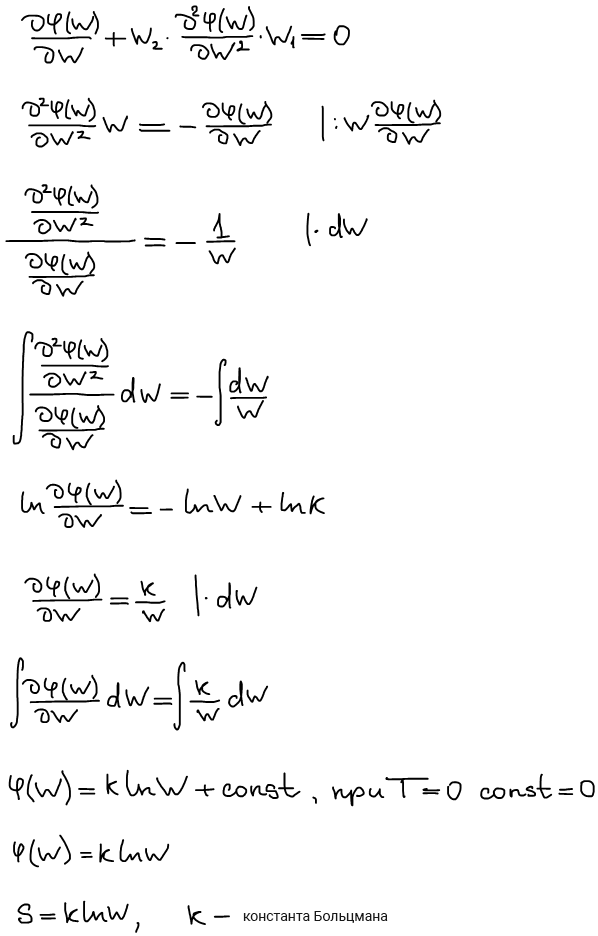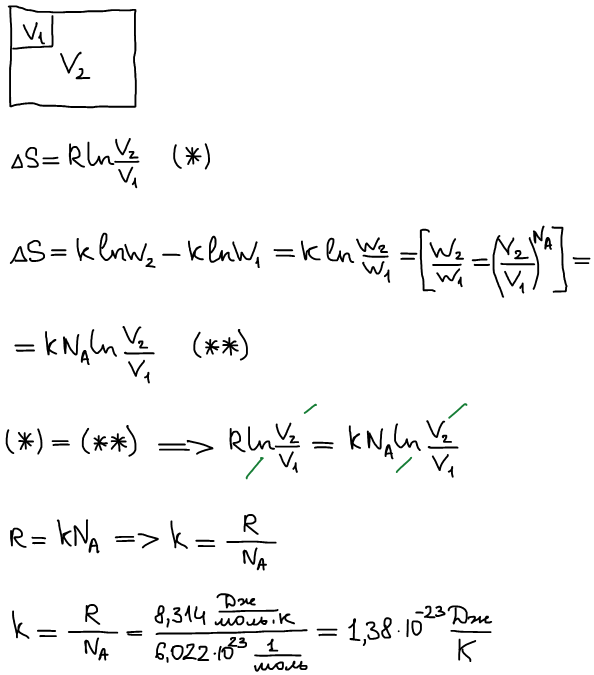Статистический смысл энтропии
1877 г. Людвиг Больцман публикует работу "Основы молекул статистики" и дает обоснование понятия энтропии. В основе лежат микро- и макросостояния.
Под микросостоянием системы понимают данный способ распределения всех молекул по всем имеющимся уровням энергии с учетом различимости молекул.
Под макросостоянием системы понимают данный способ распределения всех молекул по всем имеющимся уровням энергии без учета различимости молекул.
Модельная система: 2 уровня энергии (E1 и E2), на каждом уровне может находиться только 2 частицы.
Для того чтобы ввести микросостояния нужно различить частицы.
Термодинамическая вероятность W — число микросостояний удовлетворяющих данному микросостоянию.
где N — число частиц в системе, n — число уровней энергии.
Равнораспределение — такое распределение энергии, когда на каждом уровне находится одинаковое число частиц. Равное распределение имеет наибольшую термодинамическую вероятность.
Статистическая гипотеза Больцмана
Термодинамическая вероятность в изолированной системе всегда увеличивается при протекании самопроизвольного процесса. При этом она достигает своего максимума в состоянии равновесия.
Изолированная система всегда эволюционирует в сторону возрастания своей термодинамической вероятности.
Разобьем искомую систему на 2 части. Как определить S, если известны энтропии частиц S1 и S2.
S — экстенсивная функция;
- дифференцируем по W1, когда W2 = const
- Дифференцируем по W2, когда W1 = const